适用对象与典型场景

实验人员
当天实验当天记,文本/表单/附件一处完成,样品与物料自动关联。

实验室主管/PI
模板与审批流统一规范,跨课题沉淀可复用方法。

QA / 法规事务
电子签、审计日志、版本留痕完整,审阅与取证更高效。
关键能力概览
合规与签署闭环
提交—复核—见证—QA 释放全链可配置;电子签与审计日志完整留痕。
自由编辑 + 结构化表单
叙述与关键参数并存;字段校验、单位/范围可控,数据可统计与复用。
实验插件(连接中枢)
扫码即连样品/物料/设备,计时/计算/数据采集一站式完成并回写系统。
版本与对比
记录与模板双版本管理,差异高亮、回滚与评论审阅。
系统联动
与智研分子/样品库存/知识库/AI 助手双向衔接,减少二次录入。
产品亮点
获取专属演示合规有据可审
电子签+审计日志+版本留痕,审阅链路清晰,取证不再临时补材料。
记录既可写又可算
自由叙述与结构化表单合一,关键参数强制采集、可统计。
现场一屏完成
实验插件把扫码、计时、计算与数据采集拉到同一界面,免抄录。
记录与对象天然连通
样品/物料/设备/序列方案一键关联,消耗与批次自动回写。
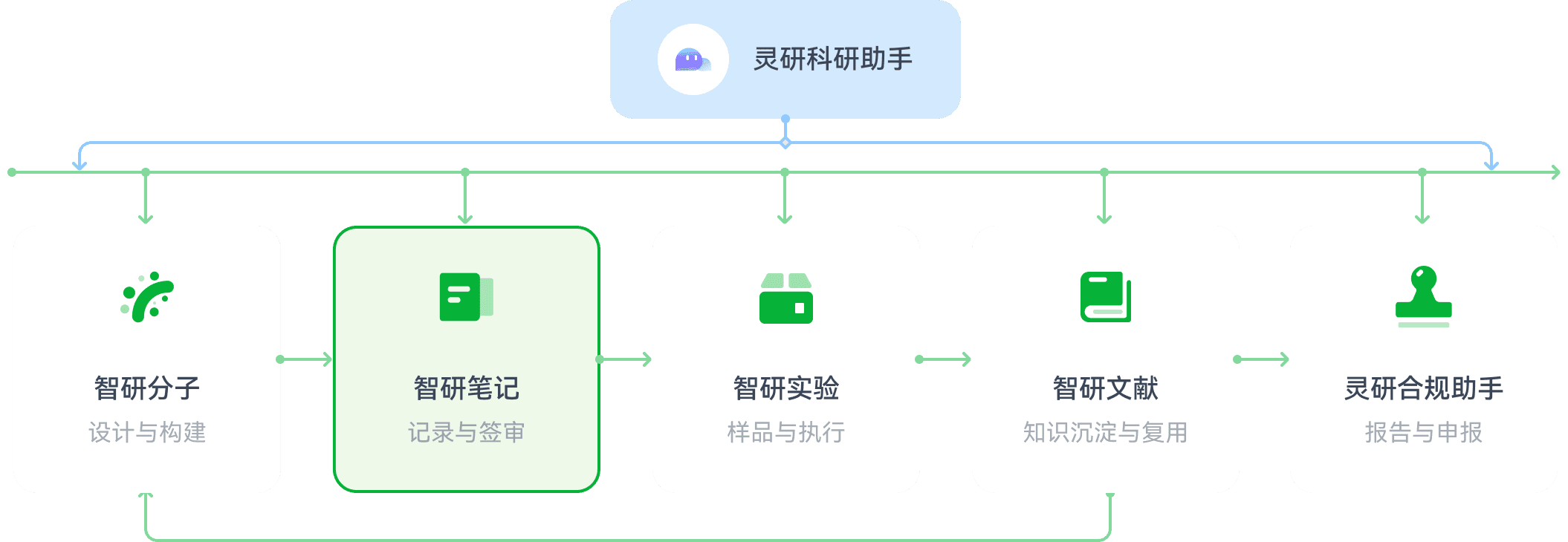
与其他产品的协同
分段式提交与签审(企业版)
一篇 ELN 可按章节/步骤逐段提交:每段单独进入签审流,已通
过的段落自动锁定,未通过段落可定向退回重写,不影响整篇进
度,
多角色串签
作者 → 复核 → 见证/QA(可选)等角色与顺序可配置;支持并
行/串行组合与到期提醒,职责边界清晰。
细粒度审计链
序列设计、交付追踪、上有原材料全流程溯源
签后锁定与受控解锁
段落/整篇签署后锁定;如需更改,必须走解锁→理由说明→重
签闭环,保证可追溯性与一致性。
权限与最小授权
项目/记录/段落/附件多级权限可配;导出、删除等高风险操作
需权限且留痕。
客户成功案例
挑战
公司细胞治疗产品面临多中心生产和严苛的GMP合规与审计要求,传统记录方式难以保证数据完整性及应对全球监管审查。
解决方案
采用「智研笔记」模块,利用其分段式提交与签审功能,将冗长的生产SOP拆解并行处理,并通过细粒度审计链确保每一步操作都可追溯、可审计,完全符合FDA 21 CFR Part 11等法规。
成果
实现了跨中心标准化记录与实时同步,批次记录审查效率提升60%,为IND申报提供了完整可靠的电子数据包,审计准备时间减少80%。
客户证言
"“「智研笔记」是我们应对全球监管审查的战略基础设施,为产品商业化上市提供了基础保障。”"

